Informationen für Mediziner
Grundlagen
Der Albumin-Funktionstest bietet die Möglichkeit, auf schnelle und einfache Weise zu überprüfen, ob die Funktionalität des Albumins als Transportprotein durch pathophysiologische Veränderungen beeinträchtigt ist. Verschiedene Module des Tests ermöglichen die diagnostische Nutzung bei unterschiedlichen Erkrankungen, wie Krebs, Lebererkrankungen und Sepsis.
Das Modul zur Krebsdiagnostik für die Beurteilung maligner Prozesse ist beim Deutschen Institut für Medizinische Dokumentation und Information (DIMDI) als “sonstiger Tumormarker” registriert. Die Diagnostik von Sepsis und Lebererkrankungen erfolgt derzeit im Rahmen klinischer Studien.
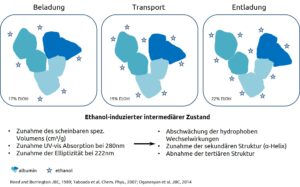
Der Albumin-Funktionstest beruht auf der Bestimmung von Konformationsänderungen des Albuminmoleküls, diese werden durch Änderungen in seiner Bindungskapazität gegenüber Fettsäuren detektiert. Die Zugabe unterschiedlicher Mengen an Ethanol induziert Veränderungen der tertiären Struktur des Albuminmoleküls im Sinne einer Öffnung. Eine Analyse der Fettsäurebindung der drei Zustände ermöglicht die Berechnung verschiedener diagnostischer Parameter (s.u.).
Das Albumin dient im Blut unter anderem als Transportprotein für wasserunlösliche Substanzen wie Fettsäuren, Vitamine und Spurenelemente sowie Metabolite und Pharmaka. So können die von Tumorzellen ins Blut abgegebenen Peptidfragmente oder Lipide an das Albumin binden (Lowenthal et al. 2005, Mehta et al. 2003, Xu et al. 1998) und bewirken dadurch eine veränderte Fettsäurebindung. Bei Patienten mit Lebererkrankungen wird dies durch eine erhöhte Toxinbelastung bewirkt (Jalan et al., 2009).
Diese veränderte Fettsäurebindung kann mit Hilfe der Elektronenspinresonanz (ESR) gemessen werden. Dafür werden einer Blutserumprobe radikaltragende Fettsäuren zugegeben und deren Bindung an das Albumin mit der ESR untersucht. Aus dem ESR-Spektrum der Serumprobe können Aussagen über die Bindungskapazität des Albumins gewonnen werden.

Da die Fettsäuren unterschiedliche Bindungseigenschaften aufweisen, zeigt das ESR-Spektrum mehrere Komponenten. In der Abbildung sind die Zerlegung eines solchen gemessenen ESR-Spektrums und die damit verbundenen Bindungsmodi dargestellt.
Aus den Komponenten des ESR-Spektrums können Bindungskonstanten, Bindungskapazitäten und biophysikalische Parameter ermittelt werden. Im Krebs-Modul werden daraus eine integrale Diskriminierungs-Funktion (DR – diagnostisches Resultat) und im Leber- bzw. Sepsis-Modul die Transportparameter berechnet.
Anwendungsgebiete
Der Albumin-Funktionstest eignet sich zur Kontrolle des therapeutischen Effektes bei einer bekannten Krebserkrankung. Ebenso ist die frühzeitige Erkennung von Rezidiven nach abgeschlossener Krebstherapie möglich. In Abhängigkeit der Lokalisation zeigt der Albumin-Funktionstest eine hohe Spezifität (ca. 90%) und Sensitivität (90%) (Seidel et al. 2005, Kazmierczak et al. 2006, Gurachevsky et al. 2008, Gelos et al. 2010, Moergel et al. 2012).
Der Albumin-Funktionstest ist für die Früherkennung von Krebs bei Risikogruppen anwendbar. Diese sind zum Beispiel Personen, die vermehrt Kontakt zu potentiell krebsauslösenden Stoffen haben oder in deren Familie gehäuft Krebserkrankungen aufgetreten sind. Da der Albumin-Funktionstest derzeit noch keine Aussage zur Lokalisation der Krebserkrankung treffen kann, ist die Untersuchung von nicht Risikopersonen mit dem Problem verbunden, welche Folgeuntersuchungen bei einem krebspositiven Befund nötig sind.
Die Diagnostik von Sepsis und Lebererkrankung erfolgt derzeit im Rahmen klinischer Studien.
Analysevoraussetzungen
Für eine einwandfreie Analyse benötigen wir:
• Mindestens 2 ml Vollblut bei ca. 8°C gelagert. Dieses sollte binnen 24 h nach der Abnahme zur
Analyse bei der MedInnovation GmbH eingetroffen sein.
• “Reines” (zentrifugiertes) Blutserum sollte innerhalb von max. 2 Tagen bei uns eintreffen. Die
Zentrifugation der Blutprobe sollte bei 1000 – 1500 x g bei Raumtemperatur erfolgen. Das Serum
bzw. EDTA-Plasma ist in ein separates und beschriftetes Röhrchen zu überführen.
• Bei der Abnahme ist zu beachten, dass kein Blutabnahmesystem mit Antikoagulantien (mit
Ausnahme von EDTA) oder Gel und -sofern möglich- kein Vakuumabnahmesystem verwendet wird.
• Nach operativen Eingriffen sowie nach einer Chemotherapie bzw. Bestrahlung, sollte ein Abstand
von 4 Wochen eingehalten werden, damit der Körper das Serumalbumin zuvor regenerieren kann.
Dies gilt auch für Erkrankungen mit entzündlichem Geschehen.
• Um korrekte Analyseergebnisse zu gewährleisten, bitten wir bei sommerlichen Temperaturen von
über 27°C von dem Versand der ungekühlten Blut- bzw. Serumproben per Post abzusehen.
• Ein leichtes Frühstück vor der Blutentnahme ist zulässig.
• Die Blutentnahme sollte vormittags erfolgen.
Wir können dem Patienten auch bei uns im Labor (Groß-Berliner Damm 151, 12487 Berlin) Blut abnehmen. Um einen reibungslosen und schnellen Ablauf zu gewährleisten, bitten wir Sie, vorher mit uns einen Termin zu vereinbaren.
Ausschlusskriterien
Akute Schübe von chronisch entzündlichen Erkrankungen wie z.B. Morbus Crohn, Colitis ulcerosa oder rheumatoide Arthritis verfälschen das Testergebnis. Es sollte ein Abstand von 4 Wochen eingehalten werden, damit der Körper das Serumalbumin zuvor regenerieren kann.
Nach operativen Eingriffen sowie nach einer Chemotherapie bzw. Bestrahlung, sollte ebenfalls ein Abstand von 4 Wochen eingehalten werden. Dies gilt auch für Erkrankungen mit entzündlichem Geschehen.
Medikamenteneinfluss
Leider ist es uns nicht möglich, sämtliche Medikamente auf ihren Einfluss auf das Ergebnis des Albumin-Funktionstests zu überprüfen. Langzeitmedikamente, die nicht abgesetzt werden können, sollten im Vorfeld genannt werden.
Bei einer Einnahme von 500 mg oder mehr Aspirin® (Acetylsalicylsäure) pro Tag sollten 4 Wochen als Abstand zum Albumin-Funktionstest eingehalten werden.
ASS 100 zur Blutverdünnung hat keinen Einfluss.
Für Medikamente, die in Zusammenhang mit einer entzündlichen Erkrankung (Gelenke, Zahn…) eingenommen werden, gilt es ebenfalls einen Abstand von 4 Wochen einzuhalten.
Interpretation der Ergebnisse
Das Testergebnis kann Ihnen innerhalb von einem Werktag übermittelt werden. Es besteht aus den vier Werten DR, BE, RTQ und DTE unter Angabe der Normalbereiche und einer Erläuterung der Werte auch in Bezug auf vorherige Ergebnisse.
Das diagnostische Resultat (DR) ist der Wert, der eine Aussage über die Wahrscheinlichkeit für das Vorliegen einer malignen Erkrankung trifft. Im Fall eines DR-Wertes kleiner als 1,0 besteht bzw. entwickelt sich mit einer hohen Wahrscheinlichkeit eine maligne Erkrankung. Bei Messung eines DR-Wertes größer als 1,0 liegt mit hoher Wahrscheinlichkeit keine maligne Erkrankung vor. Der Grenzbereich schließt Werte von 0,8 bis 1,2 ein. In diesem Grenzbereich besteht noch ein erhöhtes Risiko für das Vorhandensein einer malignen Erkrankung. Durch eine Verlaufskontrolle nach 1 bis 3 Monaten wird das Ergebnis abgesichert.
Die drei weiteren Werte, die sogenannten Transportparameter, werden bei grenzwertigem DR-Wert berücksichtigt und lassen Aussagen über eine evtl. Entzündung bzw. den Einfluss von Medikamenten auf das Testergebnis zu. (BE – Bindungseffizienz, RTQ – Reale Transportqualität, DTE – Detoxifikationseffizienz)
Bei Patienten, die einer Risikogruppe angehören und ein krebsnegatives Ergebnis erhalten haben, empfehlen wir eine jährliche Wiederholung des Tests.
Es ist wichtig, den Albumin-Funktionstest immer im Zusammenhang mit der Krankengeschichte des einzelnen Patienten sowie weiteren Untersuchungsbefunden zu betrachten. Denn neben einem aktiven malignen Wachstum (Tumorgeschehen) lösen auch andere Ereignisse – meist nur kurzfristig – auffällige DR-Werte aus: zum Beispiel Infektionen, akute Schübe von chronisch entzündlichen Erkrankungen oder operative Eingriffe sowie nach einer Chemotherapie bzw. Bestrahlung.
Vergleich mit Tumormarkern
Im Rahmen einer Studie mit Patienten mit Dickdarmerkrankungen wurde der Albumin-Funktionstest mit den Tumormarkern CEA (Carcino-Embryonales Antigen) und CA 19-9 verglichen.
Der Albumin-Funktionstest zeigt bei Krebspatienten eine deutliche Überlegenheit (91,1% richtig) im Vergleich zu den Tumormarkern CEA (45,5% richtig) und CA19-9 (27,9% richtig).

Der Albumin-Funktionstest und die konventionellen Tumormarker CEA und CA 19-9 sind bei Patienten mit Adenomen bzw. Divertikulitis in ihrer Spezifität vergleichbar.

Publikationen:
Baldassarre M, Naldi M, Zaccherini G, Bartoletti M, Antognoli A et al. (2021) Determination of Effective Albumin in Patients With Decompensated Cirrhosis: Clinical and Prognostic Implications HEPATOLOGY 2021 Mar 12. PMID: 33710623 Online ahead of print.
Moergel M, Kammerer PW, Schnurr K, Klein MO, Al-Nawas B (2012) Spin electron paramagnetic resonance of albumin for diagnosis of oral squamous cell carcinoma (OSCC). Clin Oral Investig 16: 1529-1533. PMID: 22160580
Gelos M, Hinderberger D, Welsing E, Belting J, Schnurr K, et al. (2010) Analysis of albumin fatty acid binding capacity in patients with benign and malignant colorectal diseases using electron spin resonance (ESR) spectroscopy. Int J Colorectal Dis 25: 119-127. PMID: 19644694
Rajiv Jalan, Kerstin Schnurr, Rajeshwar P Mookerjee, Sambit Sen et al. (2009) Alterations in the functional capacity of albumin in patients with decompensated cirrhosis is associated with increased mortality. HEPATOLOGY 50: 555-564. 10.1002/hep.22913
Muravsky V, Gurachevskaya T, Berezenko S, Schnurr K, Gurachevsky A. (2009) Fatty acid binding sites of human and bovine albumins: Differences observed by spin probe ESR. Spectrochim Acta A Mol Biomol Spectrosc. PMID: 19540798
Gurachevsky A, Kazmierczak SC, Jörres A, Muravsky V. (2008) Application of spin label electron paramagnetic resonance in the diagnosis and prognosis of cancer and sepsis. Clin Chem Lab Med. 46(9): 1203-10. PMID: 18783341
Kazmierczak SC, Gurachevsky A, Matthes G, Muravsky V (2006) Electron spin resonance spectroscopy of serum albumin: a novel new test for cancer diagnosis and monitoring. Clin Chem 52: 2129-2134. PMID: 16990414
Seidel P, Gurachevsky A, Muravsky V, Schnurr K, Seibt G, et al. (2005) Recognition of malignant processes with neural nets from ESR spectra of serum albumin. Z Med Phys 15: 265-272. PMID: 16422355
Literaturhinweise:
Kawashima Y, Fukutomi T, Tomonaga T, Takahashi H, Nomura F, et al. (2010) High-yield peptide-extraction method for the discovery of subnanomolar biomarkers from small serum samples. J Proteome Res 9: 1694-1705.
Taboada P, Barbosa S., Emilio Castro, Manuel Gutiérrez-Pichel, Víctor Mosquera (2007) Effect of solvation on the structure conformation of human serum albumin in aqueous–alcohol mixed solvents. Chemical Physics Volume 340: 59-68
Lowenthal MS, Mehta AI, Frogale K, Bandle RW, Araujo RP, et al. (2005) Analysis of albumin-associated peptides and proteins from ovarian cancer patients. Clin Chem 51: 1933-1945.
Simard JR, Zunszain PA, Ha CE, Yang JS, Bhagavan NV, et al. (2005) Locating high-affinity fatty acid-binding sites on albumin by x-ray crystallography and NMR spectroscopy. Proc Natl Acad Sci U S A 102: 17958-17963.
Mehta AI, Ross S, Lowenthal MS, Fusaro V, Fishman DA, et al. (2003) Biomarker amplification by serum carrier protein binding. Dis Markers 19: 1-10.
Bhattacharya AA, Grune T, Curry S (2000) Crystallographic analysis reveals common modes of binding of medium and long-chain fatty acids to human serum albumin. J Mol Biol 303: 721-732.
Peters TJ (1995) All about Albumin: Biochemistry, Genetics, and Medical Applications Academic Press, New York
Xu Y, Shen Z, Wiper DW; et al. (1998) Lysophosphatidic acid as a potential biomarker for ovarian and other gynecologic cancers. JAMA 280(8): 719-723
He XM & Carter DC (1992) Atomic structure and chemistry of human serum albumin. Nature 358(6383): 209-215.
Reed RG, Burrington CM (1989) The albumin receptor effect may be due to a surface-induced conformational change in albumin. J Biol Chem 264: 9867-9872.
Oganesyan V, Damschroder MM et al. (2014) Structural Insights into Neonatal Fc Receptor-based Recycling Mechanisms. J Biol Chem 289:7812-7824
